შედგენილია ცხოველთა ჰიგიენისა და ზოოლოგიის დეპარტამენტის თანამშრომლების მიერ:
პროფესორი, სოფლის მეურნეობის მეცნიერებათა დოქტორი
ასოცირებული პროფესორი, ვეტერინარიის მეცნიერებათა კანდიდატი
ასოცირებული პროფესორი, სოფლის მეურნეობის მეცნიერებათა კანდიდატი
წყლის წყაროს სანიტარიული და ტოპოგრაფიული კვლევა. 4
ანალიზისთვის წყლის ნიმუშის აღება. 4
წყლის ფიზიკური თვისებების შესწავლა... 5
ტემპერატურის ამოცნობა..5
გამჭვირვალობის განმარტება. 6
ფერის განმარტება. 8
სუნის განმარტება. 9
გემოსა და გემოს განსაზღვრა. 9
წყლის ქიმიური შემადგენლობის შესწავლა.. 10
წყლის დაჟანგვისუნარიანობის განსაზღვრა.. 10
წყლის რეაქციის განსაზღვრა (pH) 12
ნიტრიტების განსაზღვრა. 13
ნიტრატების განსაზღვრა. 14
წყალში სულფატების განსაზღვრა. 14
წყალში ქლორიდების განსაზღვრა. 15
წყლის სიხისტის განსაზღვრა.. 16
წყლის საერთო სიხისტის განსაზღვრა.. 17
მოსახსნელი სიხისტის განსაზღვრა. 18
მუდმივი სიხისტის განსაზღვრა. 18
წყლის გაწმენდა და დეზინფექცია.. 18
წყლის კოაგულაცია.. 19
წყლის ქლორირება.. 20
ქლორზე მოთხოვნილების განსაზღვრა წყალში.. 21
ნარჩენი ქლორის განსაზღვრა ქლორებულ წყალში. 23
წყლის დექლორირება.. 23
სანიტარული ანგარიში წყლის ხარისხის შესახებ (ჩვენი საკუთარი ანალიზის მიხედვით) 24
განაცხადი. 25
სასმელი წყლის ხარისხის შეფასება
დასკვნა სასმელი წყლის კარგი ხარისხის შესახებ კეთდება წყლის წყაროს სანიტარიული და ტოპოგრაფიული გამოკვლევის, ფიზიკური თვისებების, ქიმიური შემადგენლობის და წყლის ბაქტერიული დაბინძურების დადგენის საფუძველზე.
წყლის წყაროს სანიტარიული და ტოპოგრაფიული კვლევა
ეს კვლევა ხორციელდება წყალმომარაგების წყაროს სპეციალური რუქის გამოყენებით. ძირითადი კითხვები რუკაზე:
1. წყლის წყაროს ტიპი (ჭა, წყარო და სხვ.).
2. მშენებლობის დრო, ზომა, სიღრმე.
3. წყლის ამწევი კონსტრუქციები, ჭერი.
4. წყლის წყაროს მდებარეობა (რაიონი, ტერიტორია, რაიონი, სოფელი).
5. წყლის წყაროს მდებარეობა (ეზოში, უდაბნოში და ა.შ., გორაზე, ფერდობზე, დაბლობზე).
6. ნიადაგის ზედაპირის მოპირკეთება წყლის წყაროსთან.
7. წყლის გამოყენება.
წყლის წყაროს შემოწმებისას ყურადღება ექცევა წყლის დაბინძურების შესაძლო წყაროების იდენტიფიცირებას. გარე შემოწმების საფუძველზე ხდება წყლის წყაროს წინასწარი შეფასება.
ანალიზისთვის წყლის ნიმუშის აღება
წყლის ნიმუშის აღების ადგილი განისაზღვრება წყლის წყაროს ბუნებიდან გამომდინარე.
ღია წყლის წყაროებიდან წყლის სინჯის აღება ხდება სპეციალური აბანომეტრის აპარატით (ნახ. 1) 0,5-1 მ სიღრმეზე, ფსკერამდე არანაკლებ 10-15 სმ დაშორებით 1-2 მ. ნაპირი. ანალიზისთვის წყლის ნიმუში აღებულია შუშის ბოთლში სამიდან ხუთ ლიტრამდე.
ანალიზისთვის გაგზავნილი წყლის თითოეულ ნიმუშს ახლავს რუკა და თანდართული ჩანაწერი, რომელშიც აღნიშნულია:
1. წყლის წყაროს დასახელება, სინჯის აღების ადგილი.
2. სინჯის აღების თარიღი (წელი, თვე, დღე და საათი), ვინ აიღო ნიმუში.
3. წყლის სინჯის აღების ადგილი და პუნქტები (მანძილი ნაპირიდან, სიღრმე მდინარეში, ჭა).
4. სინჯის აღების დღეს და წინა სამი დღის ამინდის პირობები (ჰაერის ტემპერატურა, ქარი, ნალექი).
5. სინჯის აღების მეთოდი.
6. წყლის წყაროს, დაბინძურების შესაძლო წყაროების მოკლე სანიტარიული და ტოპოგრაფიული აღწერა.
7. სინჯის აღებისას წყლის ორგანოლეპტიკური შეფასების მოკლე შედეგები (ტემპერატურა, გამჭვირვალობა, ფერი, სუნი)
 |  |
გამოიყენებოდა თუ არა კონსერვი და რა გზით?
9. ანალიზის მიზანი.
ბრინჯი. 1. აბანომეტრები.
წყლის ნიმუში უნდა შემოწმდეს რაც შეიძლება სწრაფად. როგორც ბოლო საშუალება, ნებადართულია მყინვარში დაუბინძურებელი წყლის შენახვა 72 საათამდე, საკმაოდ სუფთა წყლის 48 საათის განმავლობაში და დაბინძურებული წყლის შენახვა 12 საათის განმავლობაში. თუ ზაფხულში ნიმუშის გაგზავნას ერთ დღეზე მეტი სჭირდება, რეკომენდებულია წყლის შენარჩუნება 2 მლ 25% H2S04 ხსნარის დამატებით ყოველ ლიტრ წყალზე. ბაქტერიოლოგიური გამოკვლევისთვის წყლის ნიმუშები აღებულია სტერილურ ჭურჭელში და არ ინახება.
წყლის ფიზიკური თვისებების შესწავლა
ტემპერატურის გამოვლენა
წყლის წყაროებში ტემპერატურა განისაზღვრება სკუპით ან ჩვეულებრივი თერმომეტრით, რომელიც გახვეულია მარლის რამდენიმე ფენაში. თერმომეტრი ინახება წყალში 15 წუთის განმავლობაში სინჯის აღების სიღრმეზე, რის შემდეგაც ხდება ჩვენება.
სასმელი წყლის ყველაზე ხელსაყრელი ტემპერატურაა 8-16°C.
გამჭვირვალობის განმარტება
წყლის გამჭვირვალობა დამოკიდებულია მასში შემავალი მექანიკური შეჩერებული ნივთიერებებისა და ქიმიური მინარევების რაოდენობაზე. მღვრიე წყალი ყოველთვის საეჭვოა ეპიზოოტიური და სანიტარული თვალსაზრისით. წყლის გამჭვირვალობის დასადგენად რამდენიმე მეთოდი არსებობს.
შედარების მეთოდი.საცდელი წყალი შეედინება ერთ უფერო მინის ცილინდრში, ხოლო გამოხდილი წყალი მეორეში. წყალი შეიძლება შეფასდეს, როგორც გამჭვირვალე, ოდნავ გამჭვირვალე, ოდნავ მოლურჯო, ოპალესცენტური, ოდნავ მღვრიე, მღვრიე და ძალიან მღვრიე.
 დისკის მეთოდი.წყლის გამჭვირვალობის დასადგენად უშუალოდ წყალსაცავში გამოიყენება თეთრი მინანქრის დისკი - სეჩის დისკი (ნახ. 2). როდესაც დისკი ჩაეფლო წყალში, აღინიშნება სიღრმე, რომელზედაც ის წყვეტს ხილვას და რომელზედაც კვლავ ხილული ხდება ამოღებისას. ამ ორი მნიშვნელობის საშუალო მაჩვენებელი გვიჩვენებს წყალსაცავში წყლის გამჭვირვალობას. გამჭვირვალე წყალში დისკი ხილული რჩება რამდენიმე მეტრის სიღრმეზე, ის ქრება 25-30 სმ სიღრმეზე.
დისკის მეთოდი.წყლის გამჭვირვალობის დასადგენად უშუალოდ წყალსაცავში გამოიყენება თეთრი მინანქრის დისკი - სეჩის დისკი (ნახ. 2). როდესაც დისკი ჩაეფლო წყალში, აღინიშნება სიღრმე, რომელზედაც ის წყვეტს ხილვას და რომელზედაც კვლავ ხილული ხდება ამოღებისას. ამ ორი მნიშვნელობის საშუალო მაჩვენებელი გვიჩვენებს წყალსაცავში წყლის გამჭვირვალობას. გამჭვირვალე წყალში დისკი ხილული რჩება რამდენიმე მეტრის სიღრმეზე, ის ქრება 25-30 სმ სიღრმეზე.
https://pandia.ru/text/78/361/images/image007_103.gif" alt=" ხელმოწერა:" align="left" width="307" height="34 src=">.gif" alt="ხელმოწერა:" align="left" width="307" height="51 src=">!}  ბეჭდის მეთოდი.წყლის გამჭვირვალობა შეიძლება განისაზღვროს რგოლის გამოყენებით (ნახ. 3). ამისათვის გამოიყენეთ მავთულის რგოლი 1-1,5 სმ დიამეტრით და მავთულის კვეთით 1 მმ. სახელურით დაჭერით, მავთულის რგოლი ქვეითდება ცილინდრში, წყლის ტესტირებამდე, სანამ მისი კონტურები უხილავი გახდება. შემდეგ გამოიყენეთ სახაზავი, რომ გაზომოთ სიღრმე (სმ), რომლის დროსაც რგოლი აშკარად ჩანს მოხსნისას. მისაღები გამჭვირვალობის ინდიკატორად ითვლება 40 სმ. მიღებული მონაცემები „ბეჭდით“ შეიძლება გადაიზარდოს წასაკითხად „შრიფტის მიხედვით“ (ცხრილი 1).
ბეჭდის მეთოდი.წყლის გამჭვირვალობა შეიძლება განისაზღვროს რგოლის გამოყენებით (ნახ. 3). ამისათვის გამოიყენეთ მავთულის რგოლი 1-1,5 სმ დიამეტრით და მავთულის კვეთით 1 მმ. სახელურით დაჭერით, მავთულის რგოლი ქვეითდება ცილინდრში, წყლის ტესტირებამდე, სანამ მისი კონტურები უხილავი გახდება. შემდეგ გამოიყენეთ სახაზავი, რომ გაზომოთ სიღრმე (სმ), რომლის დროსაც რგოლი აშკარად ჩანს მოხსნისას. მისაღები გამჭვირვალობის ინდიკატორად ითვლება 40 სმ. მიღებული მონაცემები „ბეჭდით“ შეიძლება გადაიზარდოს წასაკითხად „შრიფტის მიხედვით“ (ცხრილი 1).
ცხრილი 1
წყლის გამჭვირვალობის მნიშვნელობების გადაქცევა „ბეჭდით“ მნიშვნელობებად „შრიფტის მიხედვით“
მნიშვნელობა, სმ |
|||||||||||||||||||
"ბეჭდის გარშემო" | |||||||||||||||||||
"შრიფტის მიხედვით" | |||||||||||||||||||
ფერის განმარტება
ფერის განსაზღვრის მარტივი მეთოდია თეთრ ფონზე გაფილტრული საცდელი წყლის ფერის შედარება გამოხდილ წყალთან, რომელიც თანაბარი სიმაღლის ფენაშია ჩასხმული ორ უფერო ცილინდრში ბრტყელი ფსკერით.
ღია რეზერვუარებისთვის გამოიყენება სტანდარტული ფერის სასწორების ნაკრები (ნახ. 5), რომელიც მოიცავს 21 საცდელ მილს სხვადასხვა ფერის ხსნარებით - ლურჯიდან ყავისფერამდე (1-11 - ლურჯი-ყვითელი, 12-21 - ლურჯი-ყვითელი-). ყავისფერი).

ბრინჯი. 5. ფერის მასშტაბი.
რეზერვუარების ფერი ქრომატულობის შკალაზე შეიმჩნევა წყალსაცავში ჩაშვებული სეჩის დისკის ფონზე გამჭვირვალობის სიღრმეზე. ნაპოვნი წყლის ფერი განისაზღვრება შესაბამისი ტესტის მილის რაოდენობით.
საველე პირობებში წყლის ფერს ადგენენ შემდეგნაირად. 8-10 მლ საცდელი წყალი ასხამენ უფერო მინის სინჯარაში (დიამეტრის 1,5 სმ) და ადარებენ გამოხდილი წყლის ანალოგიურ სვეტს. ფერი გამოიხატება გრადუსით მე-2 ცხრილის მიხედვით.
მაგიდა 2
ფერის სავარაუდო განსაზღვრა
შეღებვა შემოწმებისას | ფერი, ხარისხი. |
|
დახვეწილი | ძალიან სუსტი მოყვითალო | |
ნატიფი ღია მოყვითალო | მოყვითალო | |
ძლივს შესამჩნევი ღია მოყვითალო | მკრთალი ყვითელი | |
ძალიან სუსტი ღია ყვითელი | ||
ღია მომწვანო | ინტენსიური ყვითელი | |
ინტენსიური ყვითელი |
სასმელი წყლის ფერი არ უნდა აღემატებოდეს 20°-ს.
სუნის გამოვლენა
წყლის სუნი 20 და 60°C ტემპერატურაზე. აიღეთ 100 მლ შესამოწმებელი წყალი სუფთა ფართოყელიან კოლბაში, დახურეთ საცობით და შეანჯღრიეთ. ღია ჭურჭელში სუნის ბუნება და ინტენსივობა განისაზღვრება ყნოსვით. შემდეგ იგივე კოლბას აფარებენ მინით, აცხელებენ 60°C-მდე, მსუბუქად ურევენ ბრუნვით და სუნის ინტენსივობას ადგენენ სუნით, ხელმძღვანელობენ 6-ბალიანი სკალათი (ცხრილი 3).
ცხრილი 3
წყლის სუნის ინტენსივობის შეფასება
სუნის სიძლიერე | მნიშვნელობა |
|
სუნი არ არის |
||
Ძალიან სუსტი | არ არის გამოვლენილი მომხმარებლის მიერ, მაგრამ გამოვლენილია გამოცდილი მკვლევარის მიერ |
|
მომხმარებელი ამას მხოლოდ მაშინ ამჩნევს, თუ სუნი მის ყურადღების ცენტრშია. |
||
აღქმადი | სუნი გამოირჩევა მომხმარებლის მიერ, რაც იწვევს მის უკმაყოფილებას |
|
გამორჩეული | სუნი, რომელიც ყურადღებას იპყრობს და წყალს უსიამოვნო დასალევად ხდის |
|
Ძალიან ძლიერი | უსიამოვნო სუნი, რაც წყალს არ სვამს |
წყლის სუნი არ უნდა აღემატებოდეს 2 ქულას.
გემოსა და გემოს განსაზღვრა
წყლის გემო დამოკიდებულია ბუნებრივი წარმოშობის ან ნივთიერებების არსებობაზე, რომლებიც წყალში შედიან მისი დაბინძურების შედეგად.
წყლის გემოს ადგენენ 20 და 60°C ტემპერატურაზე. 10-15 მლ წყალი შეჰყავთ პირში და აჩერებენ რამდენიმე წამის განმავლობაში გადაყლაპვის გარეშე. ღია რეზერვუარებიდან წყლის გემოს განსაზღვრისას, რომლებიც სანიტარიულად საეჭვოა, ნიმუში უნდა ადუღდეს 5 წუთის განმავლობაში, შემდეგ გაცივდეს 20-25°C-მდე. არსებობს 4 ძირითადი გემო: მარილიანი, ტკბილი, მწარე, მჟავე. ყველა სხვა გემოვნების შეგრძნება განისაზღვრება როგორც გემო.
გემოსა და გემოს ინტენსივობა და ხასიათი ფასდება ისევე, როგორც სუნი (ცხრილი 3). ეს მაჩვენებლები არ უნდა აღემატებოდეს 2 ქულას.
წყლის ქიმიური შემადგენლობის შესწავლა
წყლის დაჟანგვისუნარიანობის განსაზღვრა
წყალი კეთილთვისებიანად ითვლება, თუ მისი ორგანული მინარევები დაჟანგდა და გადაიქცა არაორგანულ ნაერთებად (მინერალიზებული). წყალში ორგანული ნივთიერებების პირდაპირი განსაზღვრა ტექნიკურად რთულია. მათი არსებობა შეიძლება შეფასდეს წყლის დაჟანგვის უნარით. წყლის ჟანგვიდობა გულისხმობს ჟანგბადის რაოდენობას, რომელიც საჭიროა ცხოველური და მცენარეული წარმოშობის ორგანული ნივთიერებების დასაჟანგად, რომლებიც გვხვდება 1 ლიტრ წყალში. რაც უფრო მეტი ორგანული ნივთიერებაა წყალში, მით უფრო მაღალია მისი დაჟანგვის უნარი.
წყლის დაჟანგვისუნარიანობის განსაზღვრის პრინციპი ემყარება კალიუმის პერმანგანატის თვისებას დაშლის ცხელ წყალში თავისუფალი ჟანგბადის გამოყოფით, რომელიც ჟანგავს წყალში გახსნილ ორგანულ ნივთიერებებს.
1. ბიურეტი
2. გირჩები
3. პიპეტი
4. ელექტრო ღუმელი
რეაგენტები:
1. კალიუმის პერმანგანატის KMnO4 0,01 N ხსნარი, რომლის 1 მლ მჟავე გარემოში შეიძლება გამომუშავდეს 0,08 მგ ჟანგბადი (0,316 KMnO4 1 ლიტრ გამოხდილ წყალზე).
2. ოქსილის მჟავას H2C2O4 0,01 N ხსნარი, რომლის 1 მლ დაჟანგვის დროს შთანთქავს 0,08 მგ ჟანგბადს (0,65 გ H2C2O4 1 ლიტრ გამოხდილ წყალზე).
3. 25% H2SO4 ხსნარი (1 ნაწილი H2S04 ხვედრითი წონა 1.84 განზავებულია 3 ნაწილად გამოხდილ წყალში).
ხსნარის ტიტრის დადგენა.
KMnO4 ხსნარის ტიტრი განისაზღვრება ოქსილის მჟავით.
კოლბაში ასხამენ 100 მლ გამოხდილ წყალს, უმატებენ 5 მლ 25%-იან H2SO4 ხსნარს და 8 მლ 0,01 N KMnO4 ხსნარს. კოლბაში არსებული სითხე ადუღდება 10 წუთის განმავლობაში. ამის შემდეგ კოლბას ემატება 10 მლ 0,01 N H2C2O4 ხსნარი, რაც იწვევს კოლბის მოვარდისფრო ფერის შიგთავსის გაუფერულებას. გაუფერულებული ცხელი სითხე ტიტრირდება KMnO4-ის 0,01 N ხსნარით, სანამ არ გამოჩნდება მკრთალი ვარდისფერი ელფერი.
0,01 N KM NO4 ხსნარის მილილიტრი მოხმარებული ტიტრირების პროცესამდე და მის დროს ტიტრში შეესაბამება 10 მლ 0,01 N H2C2O4 ხსნარს და გამოყოფს 0,8 მგ ჟანგბადს დაჟანგვის დროს (10´0,08 = 0,8).
ანალიზის პროგრესი:
კოლბაში ასხამენ 100 მლ საცდელ წყალს, ემატება 5 მლ 25% H2SO4 ხსნარი და 8 მლ 0,01 N KMnO4 ხსნარი.
კოლბაში არსებული სითხე ადუღდება 10 წუთის განმავლობაში. ამის შემდეგ კოლბას ემატება 10 მლ 0,01 N H2C2O4 ხსნარი. გაუფერულებული ცხელი სითხე ტიტრირდება KMnO4-ის 0,01 N ხსნარით, სანამ არ გამოჩნდება მოვარდისფრო ელფერი. მეორე ტიტრაციამდე და მის დროს მოხმარებული 0,01 N KMnO4 ხსნარის მილილიტრი რაოდენობა გამოყენებული იქნება 10 მლ H2C2O4-ის და საკვლევ წყალში შემავალი ორგანული ნივთიერებების დაჟანგვისთვის. 10 წუთის ადუღების შემდეგ წყალმა უნდა შეინარჩუნოს მკრთალი ვარდისფერი ფერი. თუ წყლის ნიმუში შეიცავს უამრავ ორგანულ ნივთიერებას, მოხარშვისას ის შეიძლება ყავისფერი გახდეს ან გაუფერულდეს. ამ შემთხვევაში შესამოწმებელი წყალი რამდენჯერმე იხსნება გამოხდილი წყლით და საბოლოო შედეგი იზრდება იმავე რაოდენობით.
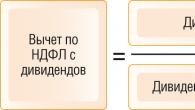
წყლის დაჟანგვის უნარი გამოითვლება ფორმულით:
![]() ,
,
სადაც: X არის წყლის სასურველი დაჟანგვისუნარიანობა მგ/ლ-ში;
V1 – KMnO4-ის მეორე ტიტრი;
V2 – KMnO4-ის პირველი ტიტრი;
K – KMnO4 ტიტრის კორექტირება;
0,08 – ჟანგბადის რაოდენობა მგ-ში გამოთავისუფლებული 1 მლ 0,01 KMnO4 ხსნარით;
V არის შემოწმებული წყლის მოცულობა.
KMnO4 ტიტრის კორექტირება ხდება H2C2O4-ის მლ-ის რაოდენობის გაყოფით KMnO4-ის მლ-ის რაოდენობაზე, რომელიც გამოიყენება ტიტრირებისთვის.
წყლის დაჟანგვა დასაშვებია 5 მგ ჟანგბადამდე 1 ლიტრზე. ორგანული ნივთიერებების სავარაუდო მასის შემცველობა 1 ლიტრ წყალში შესასწავლად მიიღება დაჟანგვის დროს მოხმარებული ჟანგბადის წონის ოდენობის 20-ზე გამრავლებით, ვინაიდან 1 მგ ჟანგბადი შეესაბამება 20 მგ ორგანულ ნივთიერებებს.
წყლის რეაქციის განსაზღვრა (pH)
წყლის რეაქციას ადგენენ მასში წითელი და ლურჯი ლაკმუსის ქაღალდების ჩაძირვით, 5 წუთის შემდეგ მათ ადარებენ გამოხდილი წყლით დასველებულ იმავე ქაღალდებს.
წითელი ფურცლის სილურჯე მიუთითებს ტუტე რეაქციაზე, ლურჯის სიწითლე მიუთითებს მჟავაზე, ხოლო თუ ქაღალდის ნაჭრების ფერი არ იცვლება, რეაქცია ნეიტრალურია. ნეიტრალურ გარემოში pH = 7, მჟავე გარემოში ნაკლებია, ტუტე გარემოში მეტია.
სასმელ წყალს უნდა ჰქონდეს ოდნავ ტუტე ან ნეიტრალური რეაქცია (6,5-დან 8-მდე).
წყლის pH მნიშვნელობის ზუსტად დასადგენად გამოიყენება კოლორიმეტრული მეთოდი ან pH მრიცხველები.
წყალში აზოტის შემცველი ნივთიერებების განსაზღვრა
წყლის დაბინძურების მნიშვნელოვანი მაჩვენებელია ამიაკის, აზოტისა და აზოტის მჟავების მარილები (ნიტრატები და ნიტრიტები).
ამიაკის განსაზღვრა
რეაგენტები:
1. როშელის მარილის 50%-იანი ხსნარი (კალიუმის ტარტრატი ნატრიუმის KNaC4H4O6 4H2O გამოხდილ წყალში).
2. ნესლერის რეაგენტი (ვერცხლისწყლის იოდიდისა და კალიუმის იოდიდის ორმაგი მარილი - НgI2 2KJ KOH ხსნარში).
ანალიზის პროგრესი.
სინჯარაში ასხამენ 10 მლ საცდელ წყალს, ემატება 0,3 მლ როშელის მარილის ხსნარი, შემდეგ ემატება 0,3 მლ ნესლერის რეაგენტი. თუ წყალში ამიაკია, 10 წუთის შემდეგ სინჯარაში ჩნდება სხვადასხვა ინტენსივობის ყვითელი ფერი, მერკურამონიუმის იოდიდის NH2Hg2JO წარმოქმნის გამო. სითხის ფერის ინტენსივობიდან გამომდინარე, მიახლოებითი დასკვნა კეთდება წყალში ამიაკის შემცველობის შესახებ მგ/ლ-ში, ცხრილი 4-ის გამოყენებით.
როდესაც წყალში ამიაკის სიუხვეა, სინჯარაში ჩნდება წითელ-ყავისფერი ნალექი.
ცხრილი 4
ამიაკის სავარაუდო განსაზღვრა
შეღებვა ნახვისას | ||
უკიდურესად სუსტი მოყვითალო | ||
უკიდურესად სუსტი მოყვითალო | სუსტად მოყვითალო | |
ძალიან ოდნავ მოყვითალო | მოყვითალო | |
ღია მოყვითალო | ||
ინტენსიური მოყვითალო-მოყავისფრო | ||
მოღრუბლული-მკვეთრი ყვითელი | ყავისფერი, მოღრუბლული ხსნარი | |
ინტენსიურად ყავისფერი, მოღრუბლული ხსნარი | ყავისფერი, მოღრუბლული ხსნარი |
ამიაკის დასაშვები შემცველობა სასმელ წყალში არის კვალი (0,02 მგ/ლ-ზე ნაკლები).
სანიტარული და ჰიგიენური კვლევა არის მეთოდების ერთობლიობა, რომელიც გამოიყენება ადამიანის სხეულზე გარე გარემოს გავლენის შესასწავლად. ამის საფუძველზე შემუშავებულია მეცნიერულად დაფუძნებული ჰიგიენური სტანდარტები. სანიტარულ და ჰიგიენურ შემოწმებას ექვემდებარება: ჰაერი, წყალი, ნიადაგი, საცხოვრებელი, საზოგადოებრივი და სამრეწველო შენობები, სამუშაო და საცხოვრებელი პირობები, ბავშვთა მოვლის საშუალებები, საკვები
სანიტარული და ჰიგიენური კვლევის მეთოდები:
სანიტარული აღწერილობითი მეთოდი:უმარტივესი და უძველესი, რომელიც იძლევა მიახლოებით წარმოდგენას შესწავლილი ობიექტის შესახებ
ორგანოლეპტიკური მეთოდები ეფუძნება:გრძნობების აღქმა და გამოიყენება ატმოსფერულ ჰაერში უცხო სუნის დასადგენად, სასმელი წყლისა და საკვები პროდუქტების ხარისხის შესაფასებლად.
ფიზიკური მეთოდები გამოიყენება:ობიექტების ზოგიერთი ფიზიკური მაჩვენებლის განსაზღვრა - ტემპერატურა, ტენიანობა, მოძრაობა, ჰაერის წნევა, ულტრაიისფერი გამოსხივება და ჰაერის იონიზაცია, სხვადასხვა ნივთიერების რადიოაქტიურობა, ტანსაცმლის ქსოვილების თბოგამტარობა; სპექტროგრაფიის, რადიომეტრიის, ფოტომეტრიის და სხვა უახლესი კვლევის მეთოდების გამოყენებით.
ფიზიკოქიმიური მეთოდების გამოყენებით განისაზღვრება შემდეგი:სიბლანტე, ელექტრული გამტარობა, დნობის წერტილი, დუღილის წერტილი და შესასწავლი ობიექტის სხვა მაჩვენებლები, კოლორიმეტრიის, პოლარიმეტრიის, ქრომატოგრაფიის, ელექტროლიზის გამოყენებით.
ქიმიური მეთოდები ძირითადად გამოიყენება:ატმოსფერული ჰაერის, სამრეწველო შენობების ჰაერის, რეზერვუარების წყლის, საკვები და საკვები პროდუქტების რაოდენობრივი ქიმიური ანალიზი
რადიოქიმიური მეთოდები გამოიყენება დასადგენად:რადიოაქტიური ნივთიერებების რაოდენობრივი შემადგენლობა გარე გარემოში
მიკროსკოპული მეთოდები გამოიყენება შესასწავლად:საკვები პროდუქტები, აეროზოლები, ჰიდროპლანქტონი, ბაქტერიოლოგიური კვლევებისთვის სინათლის, ულტრა და ელექტრონული მიკროსკოპის გამოყენებით
ბაქტერიოლოგიური მეთოდები გამოიყენება:სასმელი წყლის, საკვები პროდუქტების, აგრეთვე ჰაერის, ნიადაგის, ჩამდინარე წყლების, ტანსაცმლის, აღჭურვილობის, კვების მრეწველობის საწარმოებში, საზოგადოებებში და კვებაზე სანიტარული და ჰიგიენური კვლევები. პირველადი ყურადღება ეთმობა მიკრობების საერთო რაოდენობის განსაზღვრას და სანიტარული ინდიკატორული მიკროორგანიზმების არსებობას. ბაქტერიოლოგიურის გარდა გამოიყენება სეროლოგიური მეთოდები აგლუტინაციის, ნალექების და RSC რეაქციების გამოყენებით.
ბიოლოგიური მეთოდები:ცხოველებზე საცდელი ტესტები ტარდება მიკრობული და ქიმიური წარმოშობის ტოქსიკური ნივთიერებების დასადგენად
მიკოლოგიური მეთოდები გამოიყენება:საკვები სოკოს სახეობრივი შემადგენლობის განსაზღვრა, შხამიანი სოკოს საკვებისგან განასხვავება, პროდუქტებში პათოგენური და ტოქსიკური სოკოების გამოვლენა
ბიოქიმიური მეთოდები გამოიყენება:საკვები პროდუქტების ჰიგიენური რეგულირების პრაქტიკაში და მათი ხარისხისა და ბიოლოგიური სარგებლიანობის შეფასებისას
ჰელმინთოლოგიური მეთოდები განსაზღვრავს:ჰელმინთების, მათი კვერცხების და ლარვების არსებობა ნიადაგში, წყალში, ბოსტნეულში, ხორცსა და სხვა ობიექტებში
ფიზიოლოგიური მეთოდები გამოიყენება:ცხოველებისა და ადამიანების სხეულზე გარემო ფაქტორების გავლენის შესწავლა. მათი დახმარებით დგინდება ჰაერსა და წყალში ტოქსიკური ნივთიერებების მაქსიმალური დასაშვები კონცენტრაციების სტანდარტები. სტატისტიკური მეთოდები გამოიყენება ავადობისა და პოპულაციისა და ცხოველების ჯანმრთელობის სხვადასხვა მაჩვენებლების შესასწავლად.
თქვენი კარგი სამუშაოს გაგზავნა ცოდნის ბაზაში მარტივია. გამოიყენეთ ქვემოთ მოცემული ფორმა
სტუდენტები, კურსდამთავრებულები, ახალგაზრდა მეცნიერები, რომლებიც იყენებენ ცოდნის ბაზას სწავლასა და მუშაობაში, ძალიან მადლობლები იქნებიან თქვენი.
გამოქვეყნდა http://www.allbest.ru/
1. თემის პრაქტიკული მნიშვნელობა
სანიტარული ბაქტერიოლოგიური წყლის დეზინფექცია
წყალი ყველა ცოცხალი არსების აუცილებელი კომპონენტია და ფიზიოლოგიურად და ჰიგიენურად აუცილებელი ელემენტია. ამავდროულად, ის შეიძლება გახდეს დაავადებისა და ჯანმრთელობის პრობლემების წყარო მისი შემადგენლობის, ხარისხის ან მოხმარებული რაოდენობის ცვლილების გამო.
როდესაც წყალი იკარგება წონის ორ პროცენტზე ნაკლები რაოდენობით (1 - 1,5 ლიტრი), ჩნდება წყურვილი, 6-8% - ნახევრად გაქრობა, 10% - ჰალუცინაციები, ყლაპვის დარღვევა, 20% - სიკვდილი. ინფექციური და ჰელმინთური დაავადებების გავრცელება დაკავშირებულია წყალთან, ხოლო არაინფექციური დაავადებების სიხშირე დამოკიდებულია სასმელი წყლის მაკრო და მიკროელემენტურ შემადგენლობაზე და მავნე ქიმიკატებით მის დაბინძურებაზე. არსებობს საკმარისი ინფორმაცია წყლის ფაქტორის მნიშვნელობისა და ქოლერის გავრცელების, ტიფური ცხელების, დიზენტერიის, პარატიფოიდების A და B, ბოტკინის დაავადების, ვეილ-ვასილიევის დაავადების (იქტეროჰემორაგიული ლეპტოსპიროზი), წყლის ცხელების, ტულარემიის და მრავალი სხვა.
2. ლექციის მიზანი
1. შეიძინეთ ცოდნა წყლის ფიზიოლოგიური, ჰიგიენური და ეპიდემიოლოგიური მნიშვნელობის შესახებ. გააცნოს მოსწავლეებს წყლის ქიმიური შემადგენლობის გავლენა საზოგადოებრივ ჯანმრთელობაზე.
2. ცენტრალიზებულ წყალმომარაგებაში სასმელი წყლის ხარისხისა და წყალმომარაგების წყაროებიდან წყლის ხარისხის მოთხოვნების გათვალისწინება.
3. შეიტყვეთ ზოგადი ინფორმაცია წყლის წყაროების გამოკვლევის მეთოდოლოგიის, წყალმომარაგების წყაროს არჩევისა და წყლის სინჯების აღების წესების შესახებ სანიტარულ-ქიმიური და სანიტარიულ-ბაქტერიოლოგიური ანალიზებისთვის.
4. დაეუფლოს სასმელი წყლის ხარისხის შეფასების მეთოდოლოგიას მიკრობიოლოგიური, ტოქსიკოლოგიური და ორგანოლეპტიკური მაჩვენებლების მიხედვით.
5. გაეცანით სასმელი წყლის ხარისხის გაუმჯობესების ძირითად მეთოდებს
3. თეორიის საკითხები
წყლის ჰიგიენური, ფიზიოლოგიური და ეპიდემიოლოგიური მნიშვნელობა.
სასმელი წყლისა და წყალმომარაგების წყაროების ჰიგიენური შეფასება. წყლის დაბინძურების ინდიკატორები.
წყალმომარაგების წყაროების და წყლის მილების სანიტარული დაცვის ზონები საყოფაცხოვრებო და სასმელი მიზნებისათვის.
წყლის ფიზიკური, ქიმიური და ბაქტერიოლოგიური შემადგენლობის შესწავლა.
ენდემური დაავადებები, რომლებიც დაკავშირებულია წყალში მიკროელემენტების რაოდენობის ცვლილებასთან.
სასმელი წყლის ხარისხის გაუმჯობესების ძირითადი მეთოდებია: გამწმენდი, გაუფერულება და დეზინფექცია.
4. პრაქტიკული უნარები
1. წყლის ფიზიკური თვისებების განსაზღვრის ოსტატი მეთოდები.
2. დაეუფლეთ რამდენიმე თვისებრივ რეაქციას წყლის ქიმიური შემადგენლობის დასადგენად.
3. ისწავლეთ აქტიური ქლორის შემცველობის განსაზღვრა მათეთრებლის 1%-იან ხსნარში, ნარჩენი ქლორი და ქლორის საჭირო დოზა.
5. სასწავლო მასალა დამოუკიდებელი მუშაობისთვის
წყლის ქიმიური შემადგენლობის გავლენა ადამიანის ჯანმრთელობაზე.ბუნებრივი წყლები მნიშვნელოვნად განსხვავდება ქიმიური შემადგენლობით და მინერალიზაციის ხარისხით. ბუნებრივი წყლების მარილის შემადგენლობა წარმოდგენილია ძირითადად კათიონებით Ca, Mg, Al, Fe, K და ანიონებით HCO, Cl, NO 2, SO 4. რუსეთში წყლების მინერალიზაციის ხარისხი იზრდება ჩრდილოეთიდან სამხრეთისაკენ. წყალს, რომელიც შეიცავს 1000 მგ/ლ-ზე მეტ მინერალურ მარილებს, შეიძლება ჰქონდეს უსიამოვნო გემო (მარილიანი, მწარე-მარილიანი, შემკვრელი), შეაფერხოს სეკრეცია და გაზარდოს კუჭისა და ნაწლავების საავტომობილო ფუნქცია, უარყოფითად იმოქმედოს საკვები ნივთიერებების შეწოვაზე და გამოიწვიოს დისპეფსიური სიმპტომები. მძიმე წყლის ხანგრძლივი მოხმარება (მთლიანი სიხისტე 7 მგ-ზე მეტი - ეკვ) მიდრეკილია თირკმლის კენჭების წარმოქმნაზე.
სურგუტში წყლის მიღება მიწისქვეშა ჰორიზონტებიდან ხდება. მისი სიმტკიცე არის 1 მგ.ეკვ.ლ ფარგლებში. არსებობს ინფორმაცია რბილი წყლის მავნე ზემოქმედების შესახებ გულ-სისხლძარღვთა სისტემაზე. F.F Erisman-ის სახელობის მოსკოვის ჰიგიენის კვლევით ინსტიტუტში მიღებულმა შედეგებმა დაამტკიცა რბილი წყლის მოხმარების უარყოფითი გავლენა ადამიანის ამ სისტემაზე.
წყალში ქლორიდების მომატებულმა მდგომარეობამ შეიძლება ხელი შეუწყოს ჰიპერტენზიულ მდგომარეობას, სულფატებს - ნაწლავის აქტივობის დარღვევას, ნიტრატებს - წყალ-ნიტრატულ მეტემოგლობინემიას. ამ დაავადებას ახასიათებს დისპეფსიური სიმპტომები, ძლიერი ქოშინი და ტაქიკარდია. ჩვილებში, რომლებიც მოიხმარენ კვების ფორმულებს, რომელთა მოსამზადებლად და განზავებისთვის გამოყენებული იყო წყალი 40 მგ/ლ-ზე მეტი ნიტრატის შემცველობით, აღინიშნება ციანოზი. მეტემოგლობინის მნიშვნელოვანი პროცენტი გვხვდება სისხლში, რაც იწვევს ქსოვილების ჟანგბადის შიმშილს. უფროს ბავშვებში და მოზრდილებში ნიტრატების შემცირება და მეტემოგლობინის წარმოქმნა ხდება მცირე რაოდენობით. ეს არ ახდენს მნიშვნელოვან გავლენას მათ ჯანმრთელობაზე, მაგრამ ანემიით ან გულ-სისხლძარღვთა დაავადებებით დაავადებულ ადამიანებში შეიძლება გაზარდოს ჰიპოქსიის ეფექტი.
ადამიანის ჯანმრთელობაზე გავლენას ახდენს წყალში მიკროელემენტების შემცველობის ცვლილება: ფტორი, იოდი, სტრონციუმი, სელენი, კობალტი, მანგანუმი, მოლიბდენი და ა.შ.
მიკროელემენტები არის ქიმიური ელემენტები, რომლებიც შეიცავს მცენარეულ და ცხოველურ ორგანიზმებს მცირე რაოდენობით (ათასეული და უფრო მცირე წილადი პროცენტი). მიკროელემენტები, რომლებიც შეიცავს სხეულში ასი ათასი პროცენტის ან ნაკლები რაოდენობით, მაგალითად, ოქრო, ვერცხლისწყალი, V.I. ვერნადსკიმ მათ ულტრაელემენტები უწოდა.
ფტორის შემცველობის მატება იწვევს ფლუოროზს, შემცირება იწვევს კბილის კარიესს. იოდის ნაკლებობას თან ახლავს ფარისებრი ჯირკვლის დაზიანება. კობალტის დეფიციტით, ბავშვებში აღინიშნება მძიმე ანემიის განვითარება და პნევმონიისადმი მიდრეკილება; სპილენძის დეფიციტით, ელემენტარული ჰიპოქრომული ანემია შეიძლება განვითარდეს ბავშვებში, ორსულებში და პოსტოპერაციული ანემია. ჯუჯის ზრდა ასოცირდება თუთიის ნაკლებობასთან, ხოლო მხედველობის სიმახვილის დაქვეითება სელენის ნაკლებობასთან (მისი დაბალი კონცენტრაცია ბადურაზე). განსაკუთრებით დიდია მიკროელემენტების მნიშვნელობა ბავშვის ორგანიზმისთვის მისი ზრდისა და განვითარების ყველა ეტაპზე.
რუსეთის ტერიტორიის თითქმის 2/3 ხასიათდება იოდის ნაკლებობით, 40% - სელენით. დაუმუშავებელი სამრეწველო ჩამდინარე წყლების ჩაშვებამ შეიძლება გამოიწვიოს ღია რეზერვუარების წყალში დარიშხანის, ტყვიის, ქრომის და სხვა მავნე მინარევების ტოქსიკური კონცენტრაციის გამოჩენა.
ქიმიური დატვირთვის დონესთან ყველაზე ახლო კავშირი დამყარდა საჭმლის მომნელებელი სისტემის, შარდსასქესო სისტემის, სისხლის და სისხლმბადი ორგანოების, კანისა და კანქვეშა ქსოვილის დაავადებებთან. მაღალი დამოკიდებულება წყლის ორგანული დაბინძურების დონეზე (COD - ქიმიური მოხმარება 0 2) და ქლორორგანული ნაერთების რაოდენობაზე (OCC) დადგენილია გასტრიტის, თორმეტგოჯა ნაწლავის, არაინფექციური ენტერიტისა და კოლიტის, ღვიძლის, ნაღვლის ბუშტის დაავადებების დროს. პანკრეასი, თირკმელებისა და საშარდე გზების პათოლოგია.
ბუნებრივი წყლების რადიაქტიურობას დიდი ჰიგიენური მნიშვნელობა აქვს. ქანები შეიცავს ურანს, თორიუმს, რადიუმს, პოლონიუმს და ა.შ., ასევე რადიოაქტიურ აირებს - რადონს, თორონს. ბუნებრივი წყლების გამდიდრება რადიოაქტიური ელემენტებით განპირობებულია მინერალური ნივთიერებების გამორეცხვით, დაშლითა და გამოყოფით (რადონი, თორა). წყლის დაბინძურება ასევე ხდება მასში რადიოაქტიური ჩამდინარე წყლების შეყვანის გამო. რადიოაქტიური ელემენტების მაღალი შემცველობის წყლის გამოყენებამ შეიძლება გამოიწვიოს არასასურველი გენეტიკური შედეგები: განვითარების ანომალიები, ავთვისებიანი ნეოპლაზმები, სისხლის დაავადებები და ა.შ.
მსოფლიოს მოსახლეობის უმეტესობა მოიხმარს სასმელ წყალს (აქტივობა დაახლოებით 10-13 კური/ლ (0,4-დან 1*10"13 კური/ლ-მდე).
ცენტრალიზებული წყალმომარაგების წყაროების შერჩევა და ხარისხის შეფასება
წყალმომარაგების წყაროს არჩევისას პირველ რიგში უნდა იქნას გამოყენებული სტრატალური წნევის მიწისქვეშა წყლები. შემდეგი, მათი სანიტარული სანდოობის შემცირების მიზნით უნდა გადავიდეთ სხვა წყაროებზე: სტრატთაშორისი თავისუფალი დინების წყლები - ნაპრალი-კარსტული წყლები, ექვემდებარება მათ განსაკუთრებით საფუძვლიან ჰიდროლოგიურ კვლევას და მახასიათებლებს - მიწისქვეშა წყლები, მათ შორის ინფილტრაცია, ქვეარხი და ხელოვნურად შევსებული. ზედაპირული წყლები (მდინარეები, წყალსაცავები, ტბები, არხები).
წყლის წყაროს სანიტარული შემოწმება მოიცავს:
სანიტარიულ-ტოპოგრაფიული კვლევა;
წყლის წყაროში წყლის ხარისხისა და მისი ნაკადის განსაზღვრა;
ავადობის იდენტიფიცირება მოსახლეობასა და ზოგიერთ ცხოველურ სახეობას შორის იმ ტერიტორიაზე, სადაც მდებარეობს წყლის წყარო;
წყლის ნიმუშების აღება კვლევისთვის.
აუცილებელია გავითვალისწინოთ მონაცემები წყალმომარაგების წყაროს სანიტარული დაცვის ზონების (SPZ) ორგანიზების შესაძლებლობის შესახებ; დასავლეთის ზონის სავარაუდო საზღვრები მისი ცალკეული სარტყლების გასწვრივ; არსებული წყაროთ - მონაცემები სუს-ის მდგომარეობის შესახებ. შესწავლილია მონაცემები წყაროს წყლის დამუშავების აუცილებლობის შესახებ (დეზინფექცია, გამწმენდი, დეფერაცია და ა.შ.). გათვალისწინებულია არსებული ან შემოთავაზებული წყალმიმღების სტრუქტურის სანიტარული მახასიათებლები (წყალმიმღები, ჭა, ჭა, დრენაჟი); წყაროს დაცვის ხარისხი გარედან დაბინძურების შეღწევისგან, მიღებული ადგილების, სიღრმე, ტიპისა და დიზაინის შესაბამისობა წყალმიმღების დანიშნულებასთან და რამდენად არის შესაძლებელი საუკეთესო ხარისხის მიღება. წყალი მოცემულ პირობებში.
ცენტრალიზებული სასმელი წყალმომარაგების სისტემებით მიწოდებული სასმელი წყლის მოთხოვნები წარმოდგენილია GOST 2074-82-ში. Წყლის დალევა.
წყალმომარაგების პრაქტიკაში, მიწისქვეშა წყლების არასაკმარისი დინების გამო, ხშირად გამოიყენება ზედაპირული წყლები, რომლებიც სისტემატურად ბინძურდება საყოფაცხოვრებო, ფეკალური და სამრეწველო ჩამდინარე წყლების, გადაზიდვის, ხე-ტყის ჯომარდობის გამო და ა.შ.
ამ წყაროებიდან წყალი ექვემდებარება სავალდებულო გაწმენდას, მაგრამ იმის გამო, რომ წყლის დამუშავების შესაძლებლობები შეზღუდულია, ოფიციალური მარეგულირებელი დოკუმენტები შეიცავს ჰიგიენურ მოთხოვნებს, რომლებიც ვრცელდება წყალმომარაგების წყაროებზე.
ცხრილი 1. საყოფაცხოვრებო სასმელი წყლის ზედაპირული წყაროებიდან წყლის შემადგენლობა და თვისებები (GOST 17.1.03-77)
|
ინდექსი |
მოთხოვნები და სტანდარტები |
|
|
მცურავი მინარევები (ნივთიერებები) |
რეზერვუარის ზედაპირზე არ უნდა იყოს მცურავი ფილმები, მინერალური ზეთის ლაქები ან სხვა მინარევების დაგროვება. |
|
|
სუნი, გემო |
2 ქულამდე |
|
|
არ უნდა მოიძებნოს 20 სმ სვეტში. |
||
|
pH მნიშვნელობა |
არ უნდა აღემატებოდეს 6,5 - 8,5 pH |
|
|
მინერალური შემადგენლობა: |
||
|
მშრალი ნარჩენი |
1000 მგ/დმ 3 |
|
|
სულფატები |
||
|
ბიოქიმიური ჟანგბადის მოთხოვნა (BOD) |
წყლის საერთო მოთხოვნილება 20 0 C ტემპერატურაზე არ უნდა აღემატებოდეს 3 მგ/დმ 3 |
|
|
საერთო სიხისტე |
7 მეკვ/ლ |
|
|
ბაქტერიული შემადგენლობა |
წყალი არ უნდა შეიცავდეს ნაწლავის დაავადებების პათოგენებს. კოლიფორმული ბაქტერიების რაოდენობა (კოლის ინდექსი) არ არის 10000-ზე მეტი 1000 მლ წყალში. |
|
|
Ტოქსიკური ქიმიკატები |
არ უნდა აღემატებოდეს MPC-ს |
|
|
რკინა (მიწისქვეშა წყაროებში) |
ინფორმაცია წყლის წყაროების სანიტარული დაცვის ზონების განმსაზღვრელი ფაქტორების შესახებ, მიწისქვეშა და ზედაპირული წყაროების სანიტარიული დაცვის ზონის საზღვრების განსაზღვრის წესები, წყალმომარაგების სტრუქტურებისა და წყალსადენების სანიტარიული დაცვის ზონის საზღვრები, სანიტარიული დაცვის ზონის ტერიტორიაზე ძირითადი საქმიანობა, წყალმომარაგების წყაროების შესწავლის პროგრამა სანიტარიული დაცვის ზონის საზღვრების დასადგენად დგინდება სანიტარიული წესებით და ნორმებით (SanPiN 2.1 .4...-95). წყალმომარაგების წყაროების და წყლის მილების სანიტარული დაცვის ზონები საყოფაცხოვრებო და სასმელი მიზნებისათვის.
წყლის სინჯის აღება ლაბორატორიული ანალიზისთვის
წყლის თითოეულ ნიმუშს უნდა ჰქონდეს ნომერი და გაიგზავნოს ლაბორატორიაში თანმხლები დოკუმენტით, რომელშიც მითითებულია: წყლის წყაროს დასახელება, როდის, რომელ წერტილში და ვის მიერ იქნა აღებული ნიმუში, წყლის ტემპერატურა, ამინდის მდგომარეობა, სინჯის აღების მახასიათებლები (დან რა სიღრმე, წყლის ამოტუმბვის ხანგრძლივობა და ა.შ.) .დ.).
ღია რეზერვუარიდან წყლის სინჯები აღებულია წყლის მოხმარების უბნის ზედა და ქვედა საზღვრებზე (რეზერვუარის დინების გასწვრივ) 0,5 - 1 მ სიღრმეზე, წყალსაცავის შუაში და 10 მ მანძილზე. ბანკებიდან. წყლის სინჯები უნდა იქნას აღებული უპირველეს ყოვლისა იმ ადგილას, სადაც ხდება წყლის შეგროვება ან მოსახლეობის მიერ დაგეგმილი.
წყალს იღებენ მაღაროს ჭაბურღილებიდან 0,5 - 1 მ სიღრმეზე. ჭაბურღილებიდან წყალი პირველად იშლება ტუმბოებით და წყლის ონკანებით 5-დან 10 წუთის განმავლობაში.
სრული ქიმიური ანალიზისთვის იღებენ 5 ლიტრს. წყალი, მოკლედ - 2 ლიტრი, ქიმიურად სუფთა კონტეინერებში სხვადასხვა დიზაინის ბოთლების გამოყენებით. კონტეინერები 2-3-ჯერ ირეცხება ტესტის წყლით. აღებული წყლის ნიმუშები ექსპერტიზას ექვემდებარება მომდევნო 2-4 საათის განმავლობაში.
დიდი ხნის განმავლობაში, ნიმუში ინახება 2 მლ 25% გოგირდმჟავას დამატებით 1 ლიტრ წყალზე (დაჟანგვის და ამიაკის დასადგენად) ან 2 მლ ქლოროფორმის (შეჩერებული მყარი ნივთიერებების, მშრალი ნარჩენების, ქლორიდების, მარილების დასადგენად. აზოტოვანი და აზოტის მჟავა).
ბაქტერიოლოგიური ანალიზისთვის წყლის ნიმუშები იღებენ სტერილურ კონტეინერებში 500 მლ ოდენობით (1-3 ლიტრი პათოგენური მიკრობების დასადგენად) წყალსაცავის ზედაპირიდან 15-20 სმ სიღრმიდან ან უფრო ღრმად იმავე ადგილებში, როგორც ქიმიური. ანალიზი. კონტეინერი იხსნება სინჯის აღებამდე უშუალოდ, ხოლო ჭურჭლიდან ქაღალდის თავსახური ამოღებულია საცობთან ერთად, საცობზე ხელით შეხების გარეშე. ჩამდგარი წყლის გადინების შემდეგ წყლის ონკანის კიდე იწვება. ნიმუშები გამოკვლეულია არაუგვიანეს 2 საათისა ნებადართულია პერიოდის 6 საათამდე გახანგრძლივება, იმ პირობით, რომ წყალი ინახება ყინულში.
წყლის ფიზიკური თვისებების შესწავლა
წყლის ტემპერატურა განისაზღვრება ვერცხლისწყლის თერმომეტრით უშუალოდ წყალსაცავში ან სინჯის აღებისთანავე.
თერმომეტრი 5-10 წუთის განმავლობაში ჩაეფლო წყალში. დასალევად ოპტიმალური ტემპერატურაა 7-12 0C.
სუნი ვლინდება ოთახის ტემპერატურაზე და 60°C-მდე გაცხელებისას.
გახურების დროს სუნის განსაზღვრა ხორციელდება 250 მლ ტევადობის ფართო ყელის კოლბაში, რომელშიც ასხამენ 100 მლ შესამოწმებელი წყალი.
კოლბა დაფარულია საათის შუშით, მოთავსებულია ელექტრო ცხელ თეფშზე და აცხელებს 60°C-მდე.
შემდეგ ბრუნვითი მოძრაობებით აკანკალებენ, შუშას გვერდზე გადადებენ და სუნს სწრაფად ადგენენ.
წყლის სუნი ხასიათდება როგორც არომატული, გაფუჭებული, მერქნიანი და ა.შ. გარდა ამისა, გამოიყენება. სუნის მსგავსების ტერმინები: ქლორი, ნავთობი და ა.შ.
სუნის ინტენსივობაგანისაზღვრება 0-დან 5 ქულამდე. 0 - სუნი არ არის; 1- სუნი, რომელსაც მომხმარებელი ვერ ადგენს, მაგრამ ლაბორატორიაში ჩვეული დამკვირვებლის მიერ აღმოჩენილია; 2- მომხმარებლის მიერ ყურადღების მიქცევის შემთხვევაში შესამჩნევი სუნი; 3- სუნი, რომელიც ადვილად შესამჩნევია; 4- სუნი, რომელიც ყურადღებას იპყრობს; 5- სუნი იმდენად ძლიერია, რომ წყალი არ არის დალევა.
გემოს განსაზღვრავს მხოლოდ დეზინფექცია ან აშკარად სუფთა წყალი 20°C ტემპერატურაზე. საეჭვო შემთხვევებში წყალს ჯერ ადუღებენ 5 წუთის განმავლობაში და შემდეგ აციებენ. წყალი შეჰყავთ პირში მცირე ულუფებით, აჩერებენ რამდენიმე წამს და აგემოვნებენ მის გადაყლაპვის გარეშე. გემოვნების სიძლიერე გამოხატულიაქულებში: გემო არ არის - 0, ძალიან მცირე გემო - 1 ქულა, სუსტი - 2, შესამჩნევი -3, მკაფიო - 4 და ძალიან ძლიერი 5 ქულა. დამატებითი გემოს მახასიათებელი: მარილიანი, მწარე, მჟავე, ტკბილი; გემოვნება - თევზის, მეტალის და ა.შ.
წყლის გამჭვირვალობაგანისაზღვრება უფერო ცილინდრში, დაყოფილია სიმაღლეში სმ-ით, ბრტყელი გამჭვირვალე ფსკერით და ძირში წყლის გამოსაშვები მილით, რომელზედაც მოთავსებულია რეზინის მილი დამჭერით. Snellen შრიფტი მოთავსებულია ცილინდრის ძირის ქვეშ ისე, რომ შრიფტი ქვემოდან 4 სმ იყოს. გვერდითი მილიდან წყალი იწურება და წყლის სვეტის სიმაღლე იზომება, რაზეც შრიფტი მკაფიოდ გამოირჩევა. გამჭვირვალობა გამოიხატება სმ-ში 0,5 სმ სიზუსტით. ჯარიმაგამჭვირვალობა არის 30 სმ ან მეტი.
წყლის ფერიგანისაზღვრება უფერო ცილინდრებში ჩასხმულ გამოხდილ წყალთან შედარებით. ფერების შედარება ხდება თეთრ ფონზე. წყლის ფერი ხასიათდება შემდეგი ტერმინებითუფერო, ღია ყვითელი, ყავისფერი, მწვანე, ღია მწვანე და ა.შ. წყლის ფერის ინტენსივობა განისაზღვრება რაოდენობრივად საცდელი წყლის შედარებით სტანდარტული ხსნარების მასშტაბით თვითნებური ხარისხით. სასმელ წყალს უნდა ჰქონდეს ფერი 20-დან 35 გრადუსამდე.
ნალექი დგინდება დადებიდან ერთი საათის შემდეგ. უხსნადი შეჩერებული მყარი ნივთიერებების რაოდენობა, რომლებიც იწვევენ წყალში სიმღვრივეს, შეიძლება განისაზღვროს გრავიმეტრული მეთოდით ფილტრაციით Gooch crucible-ის გამოყენებით, რომელზეც მოთავსებულია აზბესტის ფილტრი.
შენიშვნები:
სპეციალური დამუშავების გარეშე წყალმომარაგების წყალსადენებისთვის, სანიტარიულ-ეპიდემიოლოგიური სამსახურის ორგანოებთან შეთანხმებით, ნებადართულია: მშრალი ნარჩენი 1500 მგ.ლ-მდე; საერთო სიხისტე 10 მგ-ეკვ.ლ-მდე; რკინა 1 მგ.ლ-მდე; მანგანუმი 0,5-მდე. მგ.ლ.
ქლორიდების და სულფატების კონცენტრაციების ჯამი, გამოხატული, როგორც მაქსიმალური დასაშვები კონცენტრაციის წილი თითოეული ამ ნივთიერებისთვის ცალკე, არ უნდა აღემატებოდეს 1-ს.
წყლის ორგანოლეპტიკური თვისებები
სუნი 20°C-ზე და 60°C-მდე გაცხელებისას ქულა, არაუმეტეს 2
გემო და შემდგომი გემო 20°C-ზე, ქულა, არაუმეტეს 2
ფერი, გრადუსი, არაუმეტეს 20
სიმღვრივე სტანდარტული მასშტაბით, მგ.ლ, არაუმეტეს 1,5
Შენიშვნა:სანიტარიულ-ეპიდემიოლოგიურ ზედამხედველობის ორგანოებთან შეთანხმებით ნებადართულია წყლის ფერის 35°-მდე გაზრდა, სიმღვრივის (დატბორვის პერიოდში) 2 მგ.ლ-მდე.
Ხარისხის კონტროლი:
მიწისქვეშა წყალმომარაგების წყალსადენებზე წყლის ანალიზი ტარდება მინიმუმ 4-ჯერ ექსპლუატაციის პირველი წლის განმავლობაში. (წლის სეზონების მიხედვით). მომავალში, წელიწადში ერთხელ მაინც, ყველაზე არახელსაყრელ პერიოდში, პირველი წლის შედეგების მიხედვით.
ზედაპირული წყლის მიწოდების მქონე წყალსადენებისთვის წყლის ანალიზი ტარდება თვეში ერთხელ მაინც.
ქლორისა და ოზონის წყლის დეზინფექციის მონიტორინგისას წყალსადენებზე მიწისქვეშა და ზედაპირული წყალმომარაგების წყაროებით, ნარჩენი ქლორისა და ნარჩენი ოზონის კონცენტრაცია განისაზღვრება საათში ერთხელ მაინც.
ნარჩენი ოზონის კონცენტრაცია შერევის კამერის შემდეგ უნდა იყოს 0,1 - 0,3 მგ.ლ., ამასთან, უზრუნველყოფილი იყოს კონტაქტის დრო მინიმუმ 12 წუთის განმავლობაში.
სადისტრიბუციო ქსელში სინჯების აღება ხორციელდება ქუჩების წყალშემკრები მოწყობილობებიდან, რომლებიც ახასიათებენ წყლის ხარისხს მთავარ წყალმომარაგების ხაზებში, ქუჩების გამანაწილებელი ქსელის ყველაზე ამაღლებული და ჩიხი მონაკვეთებიდან. სინჯების აღება ასევე ტარდება ყველა სახლის შიდა წყალმომარაგების ქსელების ონკანებიდან სატუმბი და ადგილობრივი წყლის ავზებით.
Წყლის დალევა. ჰიგიენური მოთხოვნები და ხარისხის კონტროლი.GOST2874 - 82
ჰიგიენური მოთხოვნები
სასმელი წყალი უნდა იყოს უსაფრთხო ეპიდემიის თვალსაზრისით, ქიმიური შემადგენლობით უვნებელი და ჰქონდეს ხელსაყრელი ორგანოლეპტიკური თვისებები.
მიკრობიოლოგიური მაჩვენებლების მიხედვით, სასმელი წყალი უნდა აკმაყოფილებდეს შემდეგ მოთხოვნებს:
მიკროორგანიზმების რაოდენობა - 3 მლ წყალი, არა უმეტეს - 100
კოლიფორმული ბაქტერიების რაოდენობა 1 ლიტრში (კოლის ინდექსი) არის არაუმეტეს 3-ისა.
წყლის ტოქსიკოლოგიური მაჩვენებლები
წყლის ხარისხის ტოქსიკოლოგიური მაჩვენებლები ახასიათებს მისი ქიმიური შემადგენლობის უვნებლობას და მოიცავს ნივთიერებების სტანდარტებს:
გვხვდება ბუნებრივ წყლებში;
დამუშავების დროს წყალს ემატება რეაგენტების სახით;
წყალმომარაგების წყაროების სამრეწველო, საყოფაცხოვრებო და სხვა დაბინძურების შედეგად.
ქიმიკატების კონცენტრაცია, რომლებიც ნაპოვნია ბუნებრივ წყლებში ან დამატებულია წყალში მისი დამუშავების დროს, არ უნდა აღემატებოდეს ქვემოთ მითითებულ სტანდარტებს:
ცხრილი 2. ქიმიური კონცენტრაციები
|
ინდიკატორის დასახელება მგ.ლ-ში, არა უმეტეს |
სტანდარტული |
|
|
ნარჩენი ალუმინი |
||
|
ბერილიუმი |
||
|
მოლიბდენი |
||
|
ნარჩენი პოლიაკრილამიდი |
||
|
სტრონციუმი |
||
|
ფტორი კლიმატური რეგიონებისთვის: |
||
ცხრილი 3. წყლის ორგანოლეპტიკური მაჩვენებლები
წყლის ქიმიური შემადგენლობის განსაზღვრა(ხარისხობრივი რეაქციები)
აქტიური რეაქცია (pH) . წყალს ასხამენ ორ სინჯარაში: ერთ-ერთში ჩაყრილია წითელი ლაკმუსის ქაღალდი, მეორეში ლურჯი ლაკმუსის ქაღალდი. ხუთი წუთის შემდეგ, ეს ქაღალდის ნაჭრები შედარებულია იმავე ნაჭრებთან; ადრე ჩაეფლო გამოხდილ წყალში. წითელი ფურცლის სილურჯე მიუთითებს ტუტე რეაქციაზე, ლურჯის სიწითლე მჟავე რეაქციაზე. თუ ქაღალდის ფერი არ შეცვლილა, მაშინ რეაქცია ნეიტრალურია.
აზოტის შემცველი ნივთიერებების განსაზღვრა.აზოტის შემცველი ნივთიერებები წყლის დაბინძურების მნიშვნელოვანი მაჩვენებელია, რადგან ისინი წარმოიქმნება ცილოვანი ნივთიერებების დაშლის დროს, რომლებიც შედიან წყლის წყაროში საყოფაცხოვრებო - ფეკალური და სამრეწველო ნარჩენებით. ამიაკი არის ცილის დაშლის პროდუქტი, ამიტომ მისი აღმოჩენა მიუთითებს ახალ დაბინძურებაზე. ნიტრიტები მიუთითებს დაბინძურების გარკვეულ ასაკზე. ნიტრატები მიუთითებს დაბინძურების ხანგრძლივ პერიოდზე. დაბინძურების ბუნება ასევე შეიძლება შეფასდეს აზოტის შემცველი ნივთიერებების მიხედვით. ტრიადის გამოვლენა (ამიაკი, ნიტრიტები და ნიტრატები) მიუთითებს წყაროსთან აშკარა პრობლემაზე, რომელიც ექვემდებარება მუდმივ დაბინძურებას.
ამიაკის ხარისხობრივი განსაზღვრაკეთდება შემდეგნაირად: ჩაასხით 10 მლ საცდელი წყალი სინჯარაში, დაამატეთ 0,2 მლ (1-2 წვეთი) როშელის მარილი და 0,2 მლ ნესლერის რეაგენტი. 10 წუთის შემდეგ ამიაკის აზოტის შემცველობა განისაზღვრება ცხრილის გამოყენებით.
ნიტრატების განსაზღვრა.სინჯარაში ასხამენ 1 მლ საცდელ წყალს, ემატება 1 კრისტალი დეფენილამინი და ფრთხილად ასხამენ, ფენად აფენს კონცენტრირებულ გოგირდმჟავას. ლურჯი რგოლის გამოჩენა მიუთითებს წყალში ნიტრატების არსებობაზე.
ნიტრიტების განსაზღვრა. 10 მლ საცდელი წყალი, 0,5 მლ გრისის რეაგენტი (10 წვეთი) ასხამენ სინჯარაში და აცხელებენ წყლის აბაზანაში 10 წუთის განმავლობაში 70-80°C ტემპერატურაზე. ნიტრიტების სავარაუდო შემცველობა განისაზღვრება ცხრილიდან.
ქლორიდების განსაზღვრა.წყაროს წყალში ქლორიდები შეიძლება იყოს ცხოველური წარმოშობის ორგანული ნივთიერებებით წყლის დაბინძურების არაპირდაპირი მაჩვენებელი. ამ შემთხვევაში მნიშვნელოვანია არა ქლორიდების კონცენტრაცია, არამედ მისი ცვლილება დროთა განმავლობაში. მარილიან ნიადაგში ქლორიდების მაღალი კონცენტრაცია შეინიშნება. ქლორიდის შემცველობა არ უნდა აღემატებოდეს 350 მგ/ლ.
თვისებრივი რეაქცია 5 მლ საცდელ წყალს ასხამენ სინჯარაში, ამჟავებენ 2-3 წვეთი აზოტის მჟავას, უმატებენ 3 წვეთ ვერცხლის ნიტრატის 10%-იან ხსნარს (ვერცხლის ნიტრატი) და ადგენენ წყლის სიმღვრივის ხარისხს. . ქლორიდის სავარაუდო შემცველობა განისაზღვრება ცხრილიდან.
სულფატების განსაზღვრა.სასმელ წყალში სულფატების გაზრდილი რაოდენობა შეიძლება ჰქონდეს საფაღარათო ეფექტი და შეცვალოს წყლის გემო. თვისებრივი რეაქცია: 5 მლ საცდელ წყალს ასხამენ სინჯარაში, ემატება 1-2 წვეთი მარილმჟავა და 3-5 წვეთი ბარიუმის ქლორიდის 5%-იანი ხსნარი. სულფატის სავარაუდო შემცველობა განისაზღვრება სიმღვრივე და ნალექი ცხრილის მიხედვით.
რკინის განსაზღვრა.ჭარბი რკინის შემცველობა წყალს აძლევს ყვითელ-ყავისფერ შეფერილობას, სიმღვრივეს და მწარე მეტალის გემოს. როდესაც ასეთი წყალი გამოიყენება საყოფაცხოვრებო მიზნებისთვის, ჟანგიანი ლაქები წარმოიქმნება თეთრეულზე და სანტექნიკის მოწყობილობებზე.
ამისთვის ხარისხობრივი განმარტებარკინა, ჩაასხით სინჯარაში 10 მლ საცდელი წყალი, დაამატეთ 2 წვეთი კონცენტრირებული მარილმჟავა და დაამატეთ 4 წვეთი ამონიუმის თიოციანატის 50%-იანი ხსნარი. მთლიანი რკინის შემცველობა განისაზღვრება ცხრილიდან.
წყლის სიხისტის განსაზღვრა.წყლის სიმტკიცე დამოკიდებულია მასში გახსნილი მაგნიუმის და კალციუმის ტუტე მიწის მარილების არსებობაზე. ზოგიერთ შემთხვევაში, წყლის სიხისტე გამოწვეულია შავი რკინის, მანგანუმის და ალუმინის არსებობით. არსებობს სიხისტის 4 ტიპი: ზოგადი, კარბონატული, მოსახსნელი და მუდმივი. წყლის სიხისტე გამოიხატება ერთ ლიტრ წყალში ხსნადი კალციუმის და მაგნიუმის მარილების მგ ეკვივალენტებში.
კარბონატული სიხისტის განსაზღვრა. 100 მლ საცდელ წყალს ასხამენ 150 მლ კოლბაში, ემატება 2 წვეთი მეთილის ფორთოხალი და ტიტრირდება 0,1 ნორმალური მარილმჟავას ხსნარით, სანამ ფერი არ გახდება ვარდისფერი. გაანგარიშება ხორციელდება ფორმულის მიხედვით:
X=(a*0.1*1000)/(v), სადაც X არის სიხისტე; ა - ტიტრირებისთვის გამოყენებული 0,1 ნ HCl ხსნარის რაოდენობა მლ-ზე; 0.1 - მჟავას ტიტრი; v არის შესამოწმებელი წყლის მოცულობა.
საერთო სიხისტის განსაზღვრა.კოლბაში 200-250 მლ შესამოწმებელი წყლის ტევადობით, დაამატეთ 5 მლ ამიაკის ბუფერული ხსნარი და 5-7 წვეთი შავი ქრომოგენის მაჩვენებელი. ტიტრარდება ნელა ენერგიული მორევით 0,1 N Trilon B ხსნარით, სანამ ღვინის წითელი ფერი არ შეიცვლება ლურჯ-მწვანედ. სიმტკიცე გამოითვლება მგ/ეკვში ფორმულის გამოყენებით:
X=(a*k*0.1*1000)/(v), სადაც X არის მთლიანი სიმტკიცე, a არის ტრილონ B-ის მოხმარება მლ-ში, k არის ტრილონ B-ის კორექტირების ფაქტორი (0.695), v არის მოცულობა. წყლის ნიმუში.
დასუფთავებადასასმელი წყლის დეზინფექცია
სანიტარული თვალსაზრისით ყველაზე ხელსაყრელია მიწისქვეშა ღრმა არტეზიული წყლები, ისევე როგორც წყაროებისა და წყაროების წყლები, რომლებიც ხშირად დიდი სიღრმეებიდან მიედინება. მათ აქვთ უკეთესი ფიზიკურ-ქიმიური თვისებები და თითქმის თავისუფალია ბაქტერიებისგან. წყლებს აქვთ დაბალი ფიზიკურ-ქიმიური თვისებები და, როგორც წესი, აქვთ მაღალი ბაქტერიული დაბინძურება. ამიტომ, ცენტრალური წყალმომარაგების დროს გამოყენებული ღია რეზერვუარებიდან წყალი საჭიროებს წინასწარ გაწმენდას და დეზინფექციას.
გაწმენდა აუმჯობესებს წყლის ფიზიკურ თვისებებს. წყალი ხდება გამჭვირვალე, თავისუფლდება ფერისა და სუნისგან. ამავდროულად, წყლიდან ამოღებულია ბაქტერიების უმეტესობა, რომლებიც წყდება, როდესაც წყალი დნება.
წყლის გასაწმენდად გამოიყენება რამდენიმე მეთოდი:
ა) დაცვა;
ბ) კოაგულაცია;
გ) ფილტრაცია.
6. დაყენება
წყლის დასალაგებლად დამონტაჟებულია სპეციალური საცობები. ამ დასახლების ავზებში წყალი ძალიან ნელა მოძრაობს და მათში რჩება 6-8 საათის განმავლობაში, ზოგჯერ მეტიც. ამ დროის განმავლობაში მასში შეჩერებული ნივთიერებების უმეტესობას აქვს დრო წყლიდან ჩამოსასვლელად, საშუალოდ 60%-მდე. ამ შემთხვევაში წყალში ძირითადად ყველაზე პატარა შეჩერებული ნაწილაკები რჩება.
7. წყლის კოაგულაცია და ფილტრაცია
დალექვისას მცირე შეჩერებული ნაწილაკების მოსაშორებლად წყალს ემატება ნალექი კოაგულანტები, სანამ ის არ მოხვდება დალექვის ავზებში. ყველაზე ხშირად, ამისათვის გამოიყენება ალუმინი (ალუმინა) - Al 2 (SO 4) 3. ალუმინის სულფატი მოქმედებს წყალში შეჩერებულ ნაწილაკებზე ორი გზით. მას აქვს დადებითი ელექტრული მუხტი, ხოლო შეჩერებულ ნაწილაკებს აქვს უარყოფითი. საპირისპიროდ დამუხტული ნაწილაკები იზიდავს ერთმანეთს, ძლიერდება და წყდება. გარდა ამისა, კოაგულანტი აყალიბებს ფანტელებს წყალში, რომლებიც დგანან, იჭერენ და მიათრევენ შეჩერებულ ნაწილაკებს ძირში. კოაგულანტის გამოყენებისას წყალი თავისუფლდება უმრავლესობის მცირე შეჩერებული ნაწილაკებისგან და დალექვის დრო შეიძლება შემცირდეს 3-4 საათამდე. თუმცა, ამავდროულად, ზოგიერთი უმცირესი შეჩერებული ნივთიერება და ბაქტერია ჯერ კიდევ რჩება წყალში, რომლის მოსაშორებლად გამოიყენება წყლის ფილტრაცია ქვიშის ფილტრებით. როდესაც ფილტრი გამოიყენება, ქვიშის ზედაპირზე იქმნება ფილმი, რომელიც შედგება იგივე შეჩერებული ნაწილაკებისგან და კოაგულანტის ფანტელებისგან. ეს ფილმი იჭერს შეჩერებულ ნაწილაკებს და ბაქტერიებს. ქვიშის ფილტრები საშუალოდ ინარჩუნებენ ბაქტერიების 80%-მდე.
წყლის ნარჩენი მიკროფლორისგან გასათავისუფლებლად ხდება მისი დეზინფექცია.
8. წყლის ქლორირება
წყლის დეზინფექციის რამდენიმე მეთოდი არსებობს. ყველაზე გავრცელებული მეთოდია ქლორირება - წყლის დეზინფექცია გაუფერულების ან აირისებრი ქლორის გამოყენებით.
დიდი პრაქტიკული მნიშვნელობა აქვს წყლის კოაგულაციისა და ქლორირების ლაბორატორიულ კონტროლს. უპირველეს ყოვლისა, აუცილებელია ამ წყლის გაწმენდისა და დეზინფექციისთვის საჭირო კოაგულანტისა და ქლორის დოზების განსაზღვრა, რადგან სხვადასხვა წყალს სჭირდება ამ ნივთიერებების სხვადასხვა რაოდენობა.
წყლის შედედება ალუმინის სულფატით
როგორც უკვე აღვნიშნეთ, წყლის შედედების ყველაზე გავრცელებული მეთოდია მისი დამუშავება ალუმინის სულფატით.
კოაგულაციის პროცესი შედგება იმისგან, რომ ალუმინის ხსნარი, წყალში დამატებისას, რეაგირებს კალციუმის და მაგნიუმის ბიკარბონატულ მარილებთან (ბიკარბონატები) და მათთან ერთად ქმნის ალუმინის ოქსიდის ჰიდრატს ფანტელების სახით. რეაქცია მიმდინარეობს განტოლების მიხედვით:
Al 2 (SO 4) 3 + 3Ca (HCO 3) 2 = 2A1 (OH) 3 + 3CaSO 4 + 6C0 2
კოაგულანტის საჭირო დოზა ძირითადად დამოკიდებულია წყლის კარბონატული (მოხსნადი) სიხისტის ხარისხზე. რბილ წყალში, რომლის მოსახსნელი სიმტკიცე 4-5°-ზე ნაკლებია, კოაგულაციის პროცესი კარგად არ მიმდინარეობს, რადგან აქ წარმოიქმნება პატარა ალუმინის ჰიდრატის ბლოკები. ასეთ შემთხვევებში საჭიროა წყალში სოდა ან ცაცხვი დავამატოთ (გაიზარდოს მოსახსნელი სიხისტე), რათა უზრუნველყოფილი იყოს საკმარისი რაოდენობის ფანტელების წარმოქმნა. კოაგულანტის დოზის არჩევას დიდი პრაქტიკული მნიშვნელობა აქვს, რადგან თუ კოაგულანტის დოზა არასაკმარისია, წარმოიქმნება რამდენიმე ფანტელი ან არ არის კარგი წყლის გამწმენდი ეფექტი; ჭარბი კოაგულანტი წყალს მჟავე გემოს აძლევს. გარდა ამისა, შესაძლებელია წყლის შემდგომი დაბინდვა ფანტელების წარმოქმნის გამო.
9. კოაგულანტის დოზის არჩევა
პირველი ეტაპი არის მოსახსნელი სიხისტის განსაზღვრა. აიღეთ 100 მლ სატესტო წყალი, დაამატეთ 2 წვეთი მეთილის ფორთოხალი და ტიტრათ 0,1 N HCL-ით, სანამ ვარდისფერი ფერი არ გამოჩნდება. მოსახსნელი სიხისტე გამოითვლება შემდეგნაირად: HCL-ის მლ (0,1 N) რაოდენობა, რომელიც გამოიყენება 100 მლ წყლის ტიტრირებისთვის, მრავლდება 2,8-ზე. კოაგულანტის დოზის ზუსტად დასადგენად მიზანშეწონილია 1% ალუმინის ხსნარის დოზების მიღება მოსახსნელი (კარბონატული) წყლის სიხისტის მნიშვნელობის შესაბამისად. ალუმინის სულფატის დოზების გამოსათვლელი ცხრილი გვიჩვენებს ურთიერთობას კოაგულანტის დოზას შორის, რომელიც შეიძლება აღმოიფხვრას სიხისტით, ასევე ნაჩვენებია მშრალი კოაგულანტის რაოდენობა, რომელიც საჭიროა მოცემულ შემთხვევაში 1 ლიტრი წყლის კოაგულაციისთვის. კოაგულაცია ტარდება 3 ჭიქაში. 1% ალუმინის ხსნარის დოზა, რომელიც შეესაბამება წყლის მოსახსნელ სიმტკიცეს, ემატება პირველ ჭიქას 200 მლ ტესტის წყლით, ხოლო კოაგულანტის უფრო მცირე დოზები ემატება თანმიმდევრულად დანარჩენ ორ ჭიქას. დაკვირვების დრო 15 წუთია. შეარჩიეთ კოაგულანტის უმცირესი დოზა, რომელიც იძლევა ფანტელების ყველაზე სწრაფ წარმოქმნას და მათ დაბინძურებას. მაგალითი: მოსახსნელი წყლის სიხისტე არის 7°. ცხრილის მიხედვით, სიხისტის ეს მნიშვნელობა შეესაბამება 1% ალუმინის ხსნარის დოზას, 5,6 მლ თითო ჭიქა 200 მლ წყალს, რომელიც ემატება პირველ ჭიქას, ხოლო მეორე ჭიქას ემატება 6° სიხისტის შესაბამისი დოზა. - 4,8 მლ, ხოლო მესამე ჭიქამდე - 4 მლ. მინა, რომელშიც საუკეთესო კოაგულაცია ხდება, აჩვენებს 1% ალუმინის ხსნარის დოზას, რომელიც საჭიროა 200 მლ წყალზე, რომელიც იმავე ცხრილის მიხედვით გარდაიქმნება მშრალ ალუმინის სულფატად გ 1 ლიტრზე.
10. წყლის ქლორირება
არსებობს ქლორირების 2 მეთოდი:
* ქლორის ნორმალური დოზები, წყლის ქლორის საჭიროებიდან გამომდინარე;
* ქლორის გაზრდილი დოზები (ოვერქლორირება).
წყლის დეზინფექციისთვის საჭირო ქლორის რაოდენობა დამოკიდებულია წყლის სისუფთავის ხარისხზე და, ძირითადად, ორგანული ნივთიერებებით მის დაბინძურებაზე, ასევე წყლის ტემპერატურაზე. ჰიგიენური თვალსაზრისით ყველაზე მისაღებია ქლორირება ნორმალურ დოზებში, რადგან შეყვანილი ქლორის შედარებით მცირე რაოდენობა ოდნავ ცვლის წყლის გემოს და სუნს და არ საჭიროებს წყლის შემდგომ დექლორირებას.
როგორც წესი, წყლის ქლორაციისთვის იღებენ მათეთრებელს ისეთი რაოდენობით, რომელსაც შეუძლია უზრუნველყოს 0,3-0,4 მგ/ლ ნარჩენი ქლორის არსებობა წყალში ქლორთან 30 წუთის განმავლობაში ზაფხულში და 1- ზამთარში 2 საათი. ეს რაოდენობები შეიძლება დადგინდეს ექსპერიმენტული ქლორირებით და ნარჩენი ქლორის შემდგომი განსაზღვრით დამუშავებულ წყალში.
წყლის ქლორირება ყველაზე ხშირად ხდება 1%-იანი მათეთრებელი ხსნარით.
ქლორიული ან მათეთრებელი კირი არის ჩამქრალი კირის ნარევი - კალციუმის ქლორიდი და კალციუმის ჰიპოქლორიტი: Ca(OH) 2 + CaCl 2 + CaOCl 2. კალციუმის ჰიპოქლორიტი წყალთან კონტაქტში გამოყოფს ჰიპოქლორმჟავას - HC1O. ეს ნაერთი არასტაბილურია და იშლება მოლეკულური ქლორისა და ატომური ჟანგბადის წარმოქმნით, რომელსაც აქვს ძირითადი ბაქტერიციდული ეფექტი. ქლორი, რომელიც გამოიყოფა ამ შემთხვევაში, ითვლება თავისუფალ აქტიურ ქლორად.
11. ქლორის აქტიური შემცველობის განსაზღვრა ქლორის 1%-იან ხსნარში
მათეთრებელი ხსნარებში აქტიური ქლორის განსაზღვრა ეფუძნება ქლორის უნარს, გადააადგილოს იოდი კალიუმის იოდიდის ხსნარიდან. გამოთავისუფლებული იოდის ტიტრირება ხდება 0,01 N ჰიპოსულფიტის ხსნარით.
მათეთრებელ ხსნარში აქტიური ქლორის დასადგენად კოლბაში ჩაასხით 5 მლ დასახლებული 1%-იანი მათეთრებელი ხსნარი, დაამატეთ 25-50 მლ გამოხდილი წყალი, 5 მლ 5% კალიუმის იოდიდის ხსნარი და 1 მლ გოგირდის მჟავა (1: 3). გამოთავისუფლებულ იოდის ტიტრირება ხდება 0,01 N ჰიპოსულფიტის ხსნარით, სანამ არ გახდება ოდნავ მოვარდისფრო, შემდეგ უმატებენ 10-15 წვეთ სახამებელს და ტიტრირებენ ხსნარის მთლიანად გაუფერულებამდე. 1 მლ 0,01 N ჰიპოსულფიტის ხსნარი აკავშირებს 1,27 მგ იოდს, რაც შეესაბამება 0,355 მგ ქლორს. გაანგარიშება ხორციელდება ფორმულის მიხედვით:
სადაც X არის მგ აქტიური ქლორის რაოდენობა, რომელიც შეიცავს 1 მლ 1% მათეთრებელ ხსნარს; ა - ტიტრირებისთვის გამოყენებული 0,01 N ჰიპოსულფიტის ხსნარის მლ რაოდენობა; v არის ანალიზისთვის აღებული წყლის მოცულობა.
12. ქლორის საჭირო დოზის განსაზღვრა
ექსპერიმენტულ ქლორირებაში დაახლოებით ვარაუდობენ, რომ სუფთა წყლისთვის ორგანული ნივთიერებების მაღალი შემცველობით (2-3 და თუნდაც 5 მგ აქტიური ქლორი 1 ლ-ზე) წყალს უმატებენ 1%-იან მათეთრებელ ხსნარს ისე, რომ არსებობს ჭარბი აქტიური ქლორი ტესტის წყლის ქლორაციისთვის და რჩება ნარჩენი ქლორი.
განსაზღვრის მეთოდი
200 მლ სატესტო წყალი ასხამენ 3 კოლბაში და 1% მათეთრებელ ხსნარს უმატებენ ბოთლს (რომლის 1 მლ შეიცავს დაახლოებით 2 მგ აქტიურ ქლორს). პირველ კოლბას დაუმატეთ 0,1 მლ მათეთრებელი, მეორეში 0,2 მლ, მესამეში 0,3 მლ, რის შემდეგაც წყალი ურევენ მინის ღეროებს და ტოვებენ 30 წუთის განმავლობაში. ნახევარი საათის შემდეგ კოლბებში ასხამენ კალიუმის იოდიდის, გოგირდმჟავას და სახამებლის 5%-იან ხსნარს. ფერადი სითხე ტიტრირდება 0,01 N ჰიპოსულფიტის ხსნარით და გამოითვლება ნარჩენი ქლორისა და წყლის მოხმარების რაოდენობა. გაანგარიშების მაგალითი: პირველ კოლბაში არ იყო გალურჯება, მეორეში ძლივს შესამჩნევი იყო, ხოლო მესამე კოლბაში იყო ინტენსიური შეღებვა. ნარჩენი ქლორის ტიტრირებამ მესამე კოლბაში მიიღო 1 მლ 0,01 N ჰიპოსულფიტის ხსნარი, შესაბამისად, ნარჩენი ქლორის რაოდენობაა 0,355 მგ. ქლორის მოთხოვნილება 200 მლ შესასწავლ წყალზე იქნება ტოლი: 0,6-0,355 = 0,245 მგ (თუ ვივარაუდებთ, რომ 1 მლ შეიცავს 2 მგ აქტიურ ქლორს, შემდეგ მესამე კოლბას დაემატა 0,6 მგ აქტიური ქლორი). საკვლევ წყალზე ქლორის მოთხოვნილება ტოლი იქნება: (0,245*1000)/200=1,2 მგ.
ჩვენ ვამატებთ 0,3 (საკონტროლო ნარჩენი ქლორი) 1,2 მგ-ს და ვიღებთ ქლორის საჭირო დოზას ტესტის წყლისთვის, რომელიც უდრის 1,5 მგ 1 ლიტრზე.
სტუდენტთა დამოუკიდებელი მუშაობა
1. გაეცანით ამ სახელმძღვანელოს შინაარსს.
2. მიიღეთ წყლის ნიმუში ლაბორატორიული ანალიზისთვის. კვლევის ოქმში შეიყვანეთ წყლის წყაროს დათვალიერებისას მიღებული ინფორმაცია.
3. ჩაატარეთ მოკლე ანალიზი ფიზიკური თვისებებისა და ქიმიური შემადგენლობის დასადგენად.
4. განსაზღვრეთ წყლის მთლიანი სიხისტე.
5. განსაზღვრეთ აქტიური ქლორის შემცველობა 1%-იან მათეთრებელ ხსნარში.
6. განახორციელეთ აქტიური ქლორირება და განსაზღვრეთ ქლორის საჭირო დოზა.
7. კვლევის შედეგები ჩაიწერეთ ოქმში. შეაფასეთ შესამოწმებელი წყლის ხარისხი ფიზიკური და ქიმიური მაჩვენებლებისა და წყლის წყაროს კვლევის მონაცემების საფუძველზე. გამოიტანეთ დასკვნა ამ წყლის საყოფაცხოვრებო და სასმელად გამოყენების შესაძლებლობის შესახებ.
8. წყლის წყაროს სანიტარული შემოწმების და წყლის ანალიზის მონაცემების საფუძველზე წყლის შეფასების სიტუაციური ამოცანების განხილვა.
13. შეამოწმეთ კითხვები თემაზე
1. წყლის ფიზიოლოგიური, სანიტარიულ-ჰიგიენური და ეპიდემიოლოგიური მნიშვნელობა.
2. წყალმომარაგების სხვადასხვა წყაროს ჰიგიენური მახასიათებლები.
3. მოთხოვნები სასმელი წყლის ხარისხზე (C GOST 2874-82) და წყლის ხარისხის საყოფაცხოვრებო სასმელი წყლის წყაროებიდან (GOST 17.1.3.00-77).
4. წყლის წყაროების სანიტარიული შემოწმების მეთოდოლოგია (სანიტარულ-ეპიდემიოლოგიური კვლევისა და სანიტარიულ-ტოპოგრაფიული კვლევის არსი).
5. ბიოლოგიური პროვინციებისა და ენდემური დაავადებების ცნება. ბიოლოგიურად აქტიური ელემენტები სასმელ წყალში, მათი ჰიგიენური შეფასება.
6. წყლის ანალიზის სახეები (სანიტარულ-ქიმიური, ბაქტერიოლოგიური, სრული, მოკლე და სხვ.).
7. სანიტარიულ-ქიმიური და ბაქტერიოლოგიური ანალიზებისთვის წყლის სინჯის აღების წესი.
8. წყლის ფიზიკური და ორგანოლეპტიკური თვისებების ჰიგიენური მნიშვნელობა და მათი განსაზღვრის მეთოდები (ტემპერატურა, ფერი, სუნი, გემო, გამჭვირვალობა და წყლის ნალექი დგომისას).
9. წყლის აქტიური რეაქცია, მისი სტანდარტები და განსაზღვრის მეთოდები.
10. მშრალი ნარჩენი, მისი ჰიგიენური მნიშვნელობა და დადგენის მეთოდი.
11. წყლის სიხისტის ფიზიოლოგიური და ჰიგიენური მნიშვნელობა და მისი განსაზღვრის მეთოდის არსი.
12. წყლის მოკლე სანიტარიული ანალიზის სქემა.
13. ბიოგენური ელემენტები: ამიაკის აზოტი, ნიტრიტები, ნიტრატები, მათი მნიშვნელობა და ხარისხობრივი განსაზღვრის მეთოდები.
14. ქლორიდები, მათი მნიშვნელობა და განსაზღვრის მეთოდები.
15. სულფატები, მათი მნიშვნელობა და განსაზღვრის მეთოდები.
16. რკინის მარილები, მათი მნიშვნელობა და ხარისხობრივი განსაზღვრის მეთოდი.
17. წყალში ორგანული ნივთიერებების სანიტარული მნიშვნელობა, წყალში მოხვედრის წყაროები.
18. წყლის გაწმენდის მეთოდები (დალექვა, კოაგულაცია, ფილტრაცია).
19. წყლის დეზინფექციის მეთოდები.
20. მათეთრებლის 1%-იან ხსნარში აქტიური ქლორის შემცველობის განსაზღვრა.
21. საცდელი წყლისთვის ქლორის საჭირო დოზის განსაზღვრა
ლიტერატურა
1. ლაბორატორიული გაკვეთილების გზამკვლევი კომუნალური ჰიგიენური ცოდნის შესახებ, რედ. გენგარუკა რ.დ. მოსკოვი 1990 წ.
2. კომუნალური ჰიგიენა. რედ. Akulova K.I., Vushtueva K.A., M. 1986 წ.
3. ბუშტუევა კ.ა. და სხვ. კომუნალური ჰიგიენის სახელმძღვანელო მ.1986წ.
4. ეკოლოგია, გარემოს მენეჯმენტი, გარემოს დაცვა დემინა გ.ა. მ.1995წ
5. რბილი წყლების ხარისხის გაუმჯობესება. ალექსეევი ლ.ს., გლადკოვი ვ.ა. მ., სტროიზდატი, 1994 წ.
გამოქვეყნებულია Allbest.ru-ზე
...მსგავსი დოკუმენტები
სასმელი წყლის ფიზიკურ-ქიმიური მახასიათებლები. ჰიგიენური მოთხოვნები სასმელი წყლის ხარისხზე. წყლის დაბინძურების წყაროების მიმოხილვა. სასმელი წყლის ხარისხი ტიუმენის რეგიონში. წყლის მნიშვნელობა ადამიანის ცხოვრებაში. წყლის რესურსების გავლენა ადამიანის ჯანმრთელობაზე.
კურსის სამუშაო, დამატებულია 05/07/2014
სასმელი წყლის მიწოდების პრობლემა. სასმელი წყლის დეზინფექციის ჰიგიენური ამოცანები. სასმელი წყლის დეზინფექციის რეაგენტი და ფიზიკური მეთოდები. ულტრაიისფერი დასხივება, ელექტრო პულსის მეთოდი, ულტრაბგერითი დეზინფექცია და ქლორირება.
რეზიუმე, დამატებულია 04/15/2011
უკრაინაში სასმელი წყლის ხარისხის მარეგულირებელი მარეგულირებელი ჩარჩო. წყლის ორგანოლეპტიკური და ტოქსიკოლოგიური თვისებების გათვალისწინება. სასმელი წყლის ხარისხის სტანდარტების გაცნობა აშშ-ში, მათი შედარება უკრაინულ და ევროპულ სტანდარტებთან.
რეზიუმე, დამატებულია 17/12/2011
ვერხნე-ტობოლსკის წყალსაცავში წყლის დაბინძურების წლიური დინამიკის შესწავლა. სანიტარული და ბაქტერიოლოგიური ანალიზის მეთოდები. წყლის გაწმენდის ძირითადი მეთოდები უშუალოდ წყალსაცავში. ქალაქ ლისაკოვსკში სასმელი წყლის დაბინძურების შედარებითი ანალიზი.
კურსის სამუშაო, დამატებულია 21/07/2015
მინერალიზაციის, ნიტრატების, ნიტრიტების, ფენოლების, მძიმე ლითონების გავლენა სასმელ წყალში საზოგადოებრივ ჯანმრთელობაზე. მარეგულირებელი მოთხოვნები მის ხარისხზე. წყლის დამუშავების ზოგადი ტექნოლოგიური სქემა. წყლის დეზინფექცია: ქლორირება, ოზონაცია და დასხივება.
ნაშრომი, დამატებულია 07/07/2014
პავლოდარის სხვადასხვა რაიონში სასმელი წყლის სინჯების აღება. სასმელი წყლის ხარისხის ქიმიური ანალიზი ექვსი ინდიკატორის მიხედვით. სასმელი წყლის ხარისხის მაჩვენებლების შედარებითი ანალიზის ჩატარება Gorvodokanal-ის მონაცემებთან, რეკომენდაციები წყალმომარაგების ხარისხის შესახებ.
სამეცნიერო ნაშრომი, დამატებულია 03/09/2011 წ
სასმელი წყლის ხარისხის მაჩვენებლებისა და მისი ფიზიკურ-ქიმიური მახასიათებლების ანალიზი. სასმელი წყლის ხარისხისა და მისი დაბინძურების ძირითადი წყაროების ჰიგიენური მოთხოვნების შესწავლა. წყლის მნიშვნელობა ადამიანის ცხოვრებაში, წყლის რესურსების გავლენა მის ჯანმრთელობაზე.
კურსის სამუშაო, დამატებულია 02/17/2010
სასმელი წყლის როლი საზოგადოებრივი ჯანმრთელობისთვის. წყლის ორგანოლეპტიკური, ქიმიური, მიკრობიოლოგიური და რადიოლოგიური მაჩვენებლების შესაბამისობა უკრაინის სახელმწიფო სტანდარტებისა და სანიტარიული კანონმდებლობის მოთხოვნებთან. სასმელი წყლის ხარისხის კონტროლი.
ანგარიში, დამატებულია 05/10/2009
ბუნებრივი წყლების მახასიათებლები და მათი გაწმენდა სამრეწველო საწარმოებისთვის. დანადგარების აღწერა სასმელი წყლის დეზინფექციისთვის, ულტრაიისფერი გამოსხივების გამოყენება ჩამდინარე წყლების დეზინფექციისთვის. პროცესების საფუძვლები და წყლის დარბილების მეთოდების კლასიფიკაცია.
ტესტი, დამატებულია 26/10/2010
სასმელი წყლის ფიზიკურ-ქიმიური მახასიათებლები, მისი ძირითადი წყაროები, მნიშვნელობა ადამიანის სიცოცხლესა და ჯანმრთელობაში. სასმელ წყალთან დაკავშირებული ძირითადი პრობლემები და მათი გადაჭრის გზები. გარემოსთან ადამიანის ურთიერთქმედების ბიოლოგიური და სოციალური ასპექტები.
სანიტარული და ჰიგიენური კვლევა არის მეთოდების ერთობლიობა, რომელიც გამოიყენება ჰიგიენაში ჰაერის, წყლის და სხვა გარემოს ობიექტების შემადგენლობის შესასწავლად. ამ კვლევების დახმარებით ასევე შესწავლილია გარემო ფაქტორების გავლენა ადამიანის ორგანიზმზე. სანიტარული და ჰიგიენური კვლევები შესაძლებელს ხდის პრევენციული ღონისძიებების შემუშავებას, რომლებიც მიზნად ისახავს მოსახლეობის ჯანმრთელობის დაცვას და ცხოვრების პირობების გაუმჯობესებას, ასევე ჰიგიენური სტანდარტების დაწესებას.
სანიტარიული და ჰიგიენური კვლევის უმარტივესი მეთოდი არის სანიტარული და აღწერითი. თუმცა ის არ იძლევა შესწავლილი ობიექტის სრულ სურათს. ქიმიური, რადიოქიმიური და რადიომეტრიული მეთოდები შესაძლებელს ხდის ადამიანისათვის მავნე ნივთიერებების განსაზღვრას გარემოს სხვადასხვა ობიექტებში. ჰიგიენისთვის ისეთი მნიშვნელოვანი პარამეტრების დადგენა, როგორიცაა ტემპერატურა, ტენიანობა, ჰაერის მოძრაობა და წნევა, ხმაური, ვიბრაცია, გასხივოსნებული ენერგიის ინტეგრალური ნაკადი, ჰაერის იონიზაცია, სხვადასხვა მასალის თბოგამტარობა, ზედაპირის განათება, საკვები პროდუქტების კალორიული შემცველობა და ა.შ., ფიზიკური კვლევა. მეთოდები ფართოდ გამოიყენება.
საკვები პროდუქტებისა და სასმელი წყლის შეფასებისას დიდი მნიშვნელობა აქვს ორგანოლეპტიკური კვლევის მეთოდებს (იხ. დეგუსტაცია).
სანიტარულ და ჰიგიენურ კვლევებში დიდი მნიშვნელობა აქვს სასმელი წყლისა და საკვები პროდუქტების, აგრეთვე ნიადაგის, საყოფაცხოვრებო ნივთების, ტანსაცმლისა და აღჭურვილობის ბაქტერიოლოგიურ გამოკვლევას (იხ.) კვების მრეწველობის საწარმოებში. ბაქტერიოლოგიური კვლევები ფართოდ გამოიყენება კვების მრეწველობის საწარმოებისა და საზოგადოებრივი კვების ქსელების პერსონალის შესამოწმებლად პათოგენური ბაქტერიების გადასატანად. ბაქტერიოლოგიური ანალიზისთვის ნიმუშები უნდა იქნას აღებული სტერილობის წესების დაცვით (იხ.).
ჰელმინთოლოგიური კვლევის მეთოდები (იხ.) გამოიყენება წყლის, ნიადაგის, ბოსტნეულის სანიტარულ და ჰიგიენურ გამოკვლევაში, აგრეთვე ხორცისა და ფინოზის კონტროლში. საზოგადოებრივი კვების დაწესებულებებში სანიტარული კონტროლის განხორციელებისას მნიშვნელოვანია პირადი სანიტარიული ჩანაწერების გამოყენებით შეამოწმოთ თუ არა ჰელმინთოზით დაავადებული მუშაკებს შორის და თუ აღმოჩენილია, ჩატარდა თუ არა მკურნალობა და ჩატარდა თუ არა საკონტროლო ანალიზი. კეთდება მკურნალობის შემდეგ.
სანიტარულ და ჰიგიენურ კვლევებში ბიოლოგიური მეთოდებიდან, ბიოანალიზის მეთოდი გამოიყენება მავნე მინარევების ტოქსიკურობის, სხვა მავნე ნივთიერებების არსებობის დასადგენად.
სტატისტიკურ მეთოდებს იყენებენ სანიტარულ და ჰიგიენურ კვლევებში საზოგადოებრივ ჯანმრთელობაზე გარემო ფაქტორების გავლენის შესწავლისას.
ადამიანისა და ცხოველის ორგანიზმის ფუნქციებსა და ფიზიოლოგიურ რეაქციებზე სხვადასხვა გარემო ფაქტორების გავლენის გასარკვევად, ფართოდ გამოიყენება ფიზიოლოგიური და ბიოქიმიური კვლევის მეთოდები. ეს მეთოდები ასევე გამოიყენება ატმოსფერულ ჰაერში, რეზერვუარების წყალში, სამრეწველო შენობების ჰაერში და საკვებ პროდუქტებში მავნე ნივთიერებების მაქსიმალური დასაშვები კონცენტრაციის გასამართლებლად. გარდა ამისა, ბიოქიმიური მეთოდები გამოიყენება საკვები პროდუქტებისა და მზა კერძების ბიოლოგიური სარგებლიანობის დასადგენად.